Oxidačný stres je opísaný ako poškodenie buniek spôsobené voľnými radikálmi alebo nestabilnými molekulami, ktoré môžu v konečnom dôsledku ovplyvniť zdravú funkciu. Ľudské telo vytvára voľné radikály na neutralizáciu baktérií a vírusov, avšak vonkajšie faktory, ako je kyslík, znečistenie a žiarenie, môžu často tiež produkovať voľné radikály. Oxidačný stres je spojený s mnohými zdravotnými problémami.
Oxidačný stres a iné stresory zapínajú vnútorné ochranné mechanizmy, ktoré môžu pomôcť regulovať antioxidačnú reakciu ľudského tela. Nrf2 je proteín, ktorý sníma úrovne oxidačného stresu a umožňuje bunkám chrániť sa pred vnútornými a vonkajšími faktormi. Ukázalo sa tiež, že Nrf2 pomáha regulovať gény zapojené do produkcie antioxidačných enzýmov a génov odozvy na stres. Účelom nižšie uvedeného článku je vysvetliť účinky Nrf2 pri rakovine.
Obsah
abstraktné
Dráha Keap1-Nrf2 je hlavným regulátorom cytoprotektívnych reakcií na oxidačný a elektrofilný stres. Hoci bunkové signálne dráhy spúšťané transkripčným faktorom Nrf2 zabraňujú iniciácii a progresii rakoviny v normálnych a premalígnych tkanivách, v úplne malígnych bunkách aktivita Nrf2 poskytuje rastovú výhodu zvýšením chemorezistencie rakoviny a zvýšením rastu nádorových buniek. V tomto grafickom prehľade poskytujeme prehľad o dráhe Keap1-Nrf2 a jej dysregulácii v rakovinových bunkách. Stručne tiež zhrnieme dôsledky konštitutívnej aktivácie Nrf2 v rakovinových bunkách a ako to možno využiť v génovej terapii rakoviny.
Kľúčové slová: Nrf2, Keap1, rakovina, prvok antioxidačnej odozvy, génová terapia
úvod
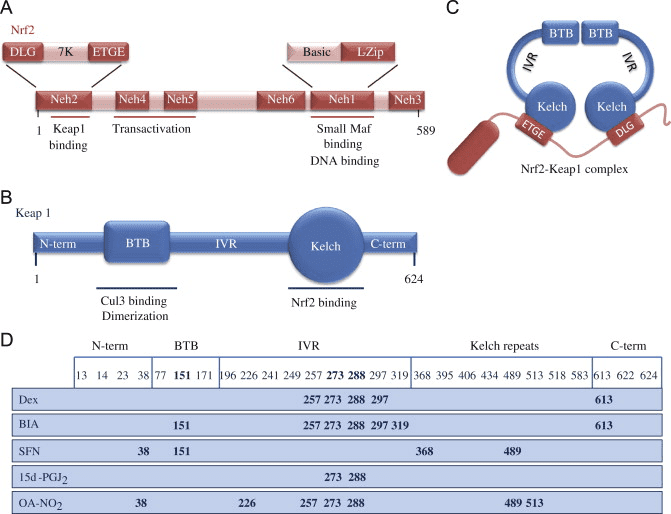
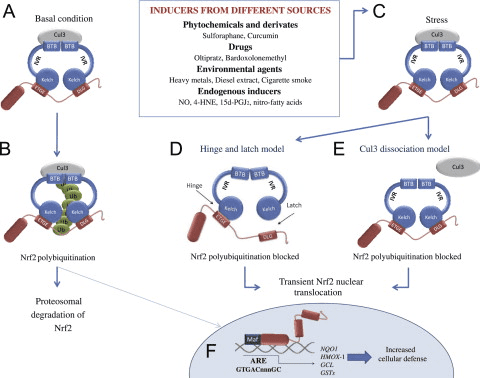
Dráha Keap1-Nrf2 je hlavným regulátorom cytoprotektívnych reakcií na endogénne a exogénne stresy spôsobené reaktívnymi formami kyslíka (ROS) a elektrofilmi [1]. Kľúčovými signálnymi proteínmi v dráhe sú transkripčný faktor Nrf2 (faktor 2 súvisiaci s erytroidným faktorom 2), ktorý sa viaže spolu s malými proteínmi Maf na prvok antioxidačnej odozvy (ARE) v regulačných oblastiach cieľových génov, a Keap1 (Kelch ECH asociačný proteín 1), represorový proteín, ktorý sa viaže na Nrf2 a podporuje jeho degradáciu prostredníctvom ubikvitínovej proteazómovej dráhy (obr. 1). Keap1 je proteín veľmi bohatý na cysteín, myšací Keap1 má celkovo 25 a ľudský 27 cysteínových zvyškov, z ktorých väčšina môže byť modifikovaná in vitro rôznymi oxidantmi a elektrofilmi [2]. Ukázalo sa, že tri z týchto zvyškov, C151, C273 a C288, hrajú funkčnú úlohu zmenou konformácie Keap1, čo vedie k jadrovej translokácii Nrf2 a následnej expresii cieľového génu [3] (obr. 1). Presný mechanizmus, ktorým cysteínové modifikácie v Keap1 vedú k aktivácii Nrf2, nie je známy, ale dva prevládajúce, ale vzájomne sa nevylučujúce modely sú (1) model „závesu a západky“, v ktorom sú modifikácie Keap1 v tiolových zvyškoch nachádzajúcich sa v IVR Keap1 narúšajú interakciu s Nrf2, čo spôsobuje nesprávne zarovnanie lyzínových zvyškov v Nrf2, ktoré už nemôžu byť polyubikvitinylované, a (2) model, v ktorom modifikácia tiolu spôsobuje disociáciu Cul3 od Keap1 [3]. V oboch modeloch je induktorom modifikovaný a na Nrf2 viazaný Keap1 inaktivovaný a následne novosyntetizované proteíny Nrf2 obchádzajú Keap1 a translokujú sa do jadra, viažu sa na ARE a riadia expresiu cieľových génov Nrf2, ako je NAD(P)H chinónoxidoreduktáza 1 (NQO1), hemoxygenáza 1 (HMOX1), glutamát-cysteín ligáza (GCL) a glutatión S transferázy (GST) (obr. 2). Okrem modifikácií tiolov Keap1, ktoré vedú k indukcii cieľového génu Nrf2, sa proteíny ako p21 a p62 môžu viazať na Nrf2 alebo Keap1, čím narúšajú interakciu medzi Nrf2 a Keap1 [1], [3] (obr. 3).
Mechanizmy aktivácie a dysregulácie Nrf2 pri rakovine
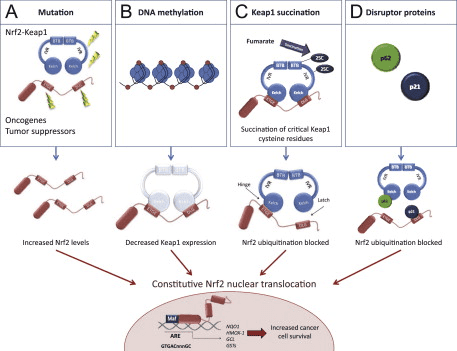
Hoci cytoprotekcia poskytovaná aktiváciou Nrf2 je dôležitá pre chemoprevenciu rakoviny v normálnych a premalígnych tkanivách, v úplne malígnych bunkách aktivita Nrf2 poskytuje rastovú výhodu zvýšením chemorezistencie rakoviny a zvýšením rastu nádorových buniek [4]. Bolo opísaných niekoľko mechanizmov, ktorými je signálna dráha Nrf2 konštitutívne aktivovaná pri rôznych rakovinách: (1) somatické mutácie v Keap1 alebo väzbovej doméne Keap1 Nrf2 narušujúce ich interakciu; (2) epigenetické umlčanie expresie Keap1 vedúce k defektnej represii Nrf2; (3) akumulácia disruptorových proteínov, ako je p62, čo vedie k disociácii komplexu Keap1-Nrf2; (4) transkripčná indukcia Nrf2 onkogénnymi K-Ras, B-Raf a c-Myc; a (5) posttranslačnú modifikáciu Keap1 cysteínov sukcinyláciou, ktorá sa vyskytuje pri familiárnom papilárnom renálnom karcinóme v dôsledku straty enzýmovej aktivity fumarát hydratázy [3], [4], [5], [6], [7], [ 8], [9], [10] (obr. 3). Konštitutívne hojný proteín Nrf2 spôsobuje zvýšenú expresiu génov zapojených do metabolizmu liečiv, čím zvyšuje odolnosť voči chemoterapeutickým liečivám a rádioterapii. Okrem toho vysoká hladina proteínu Nrf2 je spojená so zlou prognózou rakoviny [4]. Nadmerne aktívny Nrf2 tiež ovplyvňuje bunkovú proliferáciu nasmerovaním glukózy a glutamínu smerom k anabolickým dráham, ktoré zvyšujú syntézu purínov a ovplyvňujú dráhu pentózofosfátu na podporu bunkovej proliferácie [11] (obr. 4).
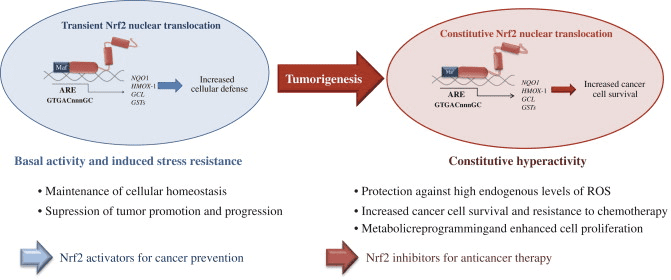
Vzhľadom na to, že vysoká aktivita Nrf2 sa bežne vyskytuje v rakovinových bunkách s nepriaznivými výsledkami, existuje potreba terapií na inhibíciu Nrf2. Bohužiaľ, v dôsledku štrukturálnej podobnosti s niektorými ďalšími členmi rodiny bZip je vývoj špecifických inhibítorov Nrf2 náročnou úlohou a doteraz bolo publikovaných len niekoľko štúdií inhibície Nrf2. Skríningom prírodných produktov Ren a spol. [12] identifikovali antineoplastickú zlúčeninu brusatol ako inhibítor Nrf2, ktorý zvyšuje chemoterapeutickú účinnosť cisplatiny. Okrem toho sa na inhibíciu Nrf3 v rakovinových bunkách použili inhibítory PI11K [13], [2] a Nrf14 siRNA [2]. Nedávno sme použili alternatívny prístup, známy ako génová terapia samovraždy rakoviny, na zacielenie rakovinových buniek s vysokými hladinami Nrf2. Lentivírusové vektory riadené Nrf2 [15] obsahujúce tymidínkinázu (TK) sa prenesú do rakovinových buniek s vysokou aktivitou ARE a bunky sa ošetria proliečivom, ganciklovirom (GCV). GCV sa metabolizuje na GCV-monofosfát, ktorý je ďalej fosforylovaný bunkovými kinázami na toxickú trifosfátovú formu [16] (obr. 5). To vedie k účinnému zabíjaniu nielen nádorových buniek obsahujúcich TK, ale aj susedných buniek v dôsledku efektu okoloidúcich [17]. Génová terapia TK/GCV regulovaná ARE môže byť ďalej posilnená kombináciou protirakovinovej chemoterapeutickej látky doxorubicínu s liečbou [16], čo podporuje názor, že tento prístup by mohol byť užitočný v spojení s tradičnými terapiami.
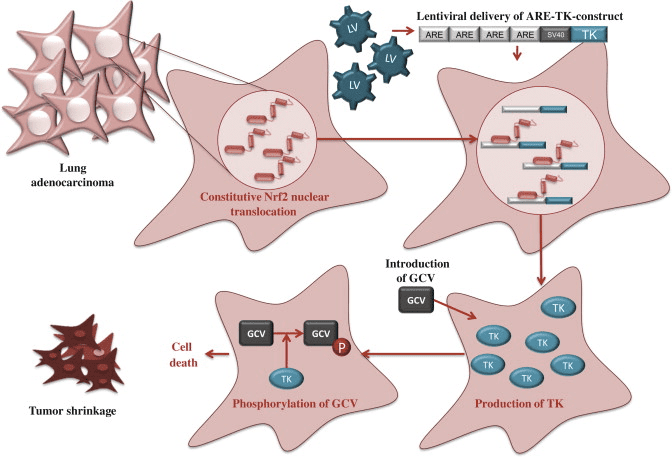

Nrf2 je hlavný regulátor, ktorý spúšťa produkciu silných antioxidantov v ľudskom tele, ktoré pomáhajú eliminovať oxidačný stres. Prostredníctvom dráhy Nrf2 sa aktivujú aj rôzne antioxidačné enzýmy, ako je superoxiddismutáza alebo SOD, glutatión a kataláza. Okrem toho niektoré fytochemikálie, ako je kurkuma, ashwagandha, bacopa, zelený čaj a ostropestrec, aktivujú Nrf2. Výskumné štúdie to zistili Aktivácia Nrf2 môže prirodzene zvýšiť ochranu buniek a obnoviť rovnováhu ľudského tela.
Dr. Alex Jimenez DC, CCST Insight
Sulforaphane a jeho účinky na rakovinu, úmrtnosť, starnutie, mozog a správanie, srdcové choroby a ďalšie
Izotiokyanáty sú niektoré z najdôležitejších rastlinných zlúčenín, ktoré môžete získať vo svojej strave. V tomto videu pre nich robím najkomplexnejší prípad, aký kedy bol vyrobený. Krátka doba pozornosti? Preskočte na svoju obľúbenú tému kliknutím na jeden z časových bodov nižšie. Úplná časová os nižšie.
Kľúčové sekcie:
- 00:01:14 – Rakovina a úmrtnosť
- 00:19:04 – Starnutie
- 00:26:30 – Mozog a správanie
- 00:38:06 – Záverečná rekapitulácia
- 00:40:27 – Dávka
Úplná časová os:
- 00:00:34 – Predstavenie sulforafanu, hlavné zameranie videa.
- 00:01:14 – Spotreba krížovej zeleniny a zníženie úmrtnosti zo všetkých príčin.
- 00:02:12 – Riziko rakoviny prostaty.
- 00:02:23 – Riziko rakoviny močového mechúra.
- 00:02:34 – Riziko rakoviny pľúc u fajčiarov.
- 00:02:48 – Riziko rakoviny prsníka.
- 00:03:13 – Hypotetické: čo ak už máte rakovinu? (intervenčné)
- 00:03:35 – Pravdepodobný mechanizmus, ktorý riadi asociatívne údaje o rakovine a úmrtnosti.
- 00:04:38 – Sulforafán a rakovina.
- 00:05:32 – Dôkazy na zvieratách ukazujúce silný účinok extraktu z výhonkov brokolice na vývoj nádoru močového mechúra u potkanov.
- 00:06:06 – Účinok priamej suplementácie sulforafanu u pacientov s rakovinou prostaty.
- 00:07:09 – Bioakumulácia izotiokyanátových metabolitov v aktuálnom prsnom tkanive.
- 00:08:32 – Inhibícia kmeňových buniek rakoviny prsníka.
- 00:08:53 – Lekcia dejepisu: Brassica bola preukázaná ako zdraviu prospešné už v starovekom Ríme.
- 00:09:16 – Schopnosť sulforafanu zvyšovať vylučovanie karcinogénov (benzén, akroleín).
- 00:09:51 – NRF2 ako genetický prepínač prostredníctvom prvkov antioxidačnej odozvy.
- 00:10:10 – Ako aktivácia NRF2 zvyšuje vylučovanie karcinogénu cez glutatión-S-konjugáty.
- 00:10:34 – Ružičkový kel zvyšuje glutatión-S-transferázu a znižuje poškodenie DNA.
- 00:11:20 – Nápoj z brokolicových klíčkov zvyšuje vylučovanie benzénu o 61 %.
- 00:13:31 – Homogenát brokolicových klíčkov zvyšuje antioxidačné enzýmy v horných dýchacích cestách.
- 00:15:45 – Spotreba krížovej zeleniny a úmrtnosť na srdcové choroby.
- 00:16:55 – Prášok z brokolicových klíčkov zlepšuje krvné lipidy a celkové riziko srdcových chorôb u diabetikov 2. typu.
- 00:19:04 – Začiatok úseku starnutia.
- 00:19:21 – Diéta obohatená o sulforafan zvyšuje životnosť chrobákov z 15 na 30 % (za určitých podmienok).
- 00:20:34 – Význam nízkeho zápalu pre dlhovekosť.
- 00:22:05 – Zdá sa, že krížová zelenina a prášok z brokolicových klíčkov znižujú množstvo zápalových markerov u ľudí.
- 00:23:40 – Rekapitulácia v polovici videa: rakovina, starnutie
- 00:24:14 – Štúdie na myšiach naznačujú, že sulforafan môže zlepšiť adaptívnu imunitnú funkciu v starobe.
- 00:25:18 – Sulforaphane zlepšil rast vlasov u myšieho modelu plešatenia. Snímka o 00:26:10.
- 00:26:30 – Začiatok sekcie mozog a správanie.
- 00:27:18 – Vplyv extraktu z brokolicových klíčkov na autizmus.
- 00:27:48 – Účinok glukorafanínu na schizofréniu.
- 00:28:17 – Začiatok diskusie o depresii (pravdepodobný mechanizmus a štúdie).
- 00:31:21 – Štúdia na myšiach s použitím 10 rôznych modelov depresie vyvolanej stresom ukazuje, že sulforafan je podobne účinný ako fluoxetín (prozac).
- 00:32:00 – Štúdia ukazuje, že priame požitie glukorafanínu u myší je podobne účinné pri prevencii depresie zo sociálneho modelu stresu.
- 00:33:01 – Začiatok sekcie neurodegenerácie.
- 00:33:30 – Sulforafán a Alzheimerova choroba.
- 00:33:44 – Sulforaphane a Parkinsonova choroba.
- 00:33:51 - Sulforaphane a Hungtingtonova choroba.
- 00:34:13 – Sulforaphane zvyšuje proteíny tepelného šoku.
- 00:34:43 – Začiatok sekcie traumatického poranenia mozgu.
- 00:35:01 – Sulforaphane podaný ihneď po TBI zlepšuje pamäť (štúdia na myšiach).
- 00:35:55 – Sulforafán a plasticita neurónov.
- 00:36:32 – Sulforaphane zlepšuje učenie v modeli diabetu typu II u myší.
- 00:37:19 – Sulforaphane a Duchennova svalová dystrofia.
- 00:37:44 – Inhibícia myostatínu vo svalových satelitných bunkách (in vitro).
- 00:38:06 – Neskoré video rekapitulácia: úmrtnosť a rakovina, poškodenie DNA, oxidačný stres a zápal, vylučovanie benzénu, kardiovaskulárne ochorenia, diabetes typu II, účinky na mozog (depresia, autizmus, schizofrénia, neurodegenerácia), dráha NRF2.
- 00:40:27 – Myšlienky na to, ako zistiť dávku brokolicových klíčkov alebo sulforafanu.
- 00:41:01 – Anekdoty o klíčení doma.
- 00:43:14 – O teplotách varenia a aktivite sulforafanu.
- 00:43:45 – Premena sulforafanu z glukorafanínu črevnými baktériami.
- 00:44:24 – Doplnky fungujú lepšie v kombinácii s aktívnou myrozinázou zo zeleniny.
- 00:44:56 – Techniky varenia a krížová zelenina.
- 00:46:06 – Izotiokyanáty ako struma.
Poďakovanie
Túto prácu podporila Fínska akadémia, Nadácia Sigrid Juselius a Fínske organizácie proti rakovine.
Záverom možno povedať, že nukleárny faktor (odvodený od erytroidov 2) podobný 2, tiež známy ako NFE2L2 alebo Nrf2, je proteín, ktorý zvyšuje produkciu antioxidantov, ktoré chránia ľudské telo pred oxidačným stresom. Ako je opísané vyššie, stimulácia dráhy Nrf2 sú štúdie na liečbu chorôb spôsobených oxidačným stresom, vrátane rakoviny. Rozsah našich informácií je obmedzený na chiropraktické a zdravotné problémy chrbtice. Ak chcete prediskutovať túto tému, neváhajte sa opýtať Dr. Jimeneza alebo nás kontaktujte na adrese�915-850-0900 .
Kurátorom je Dr. Alex Jimenez
Odkaz z:�Sciencedirect.com

Ďalšia téma diskusie: Zmiernenie bolesti kolena bez operácie
Bolesť kolena je dobre známym príznakom, ktorý sa môže vyskytnúť v dôsledku rôznych zranení a/alebo stavov kolena, vrátane�športové zranenia. Koleno je jedným z najzložitejších kĺbov v ľudskom tele, pretože je tvorené priesečníkom štyroch kostí, štyroch väzov, rôznych šliach, dvoch meniskov a chrupavky. Podľa Americkej akadémie rodinných lekárov medzi najčastejšie príčiny bolesti kolena patrí patelárna subluxácia, patelárna tendinitída alebo skokanovo koleno a Osgood-Schlatterova choroba. Hoci bolesť kolena sa s najväčšou pravdepodobnosťou vyskytuje u ľudí starších ako 60 rokov, bolesť kolena sa môže vyskytnúť aj u detí a dospievajúcich. Bolesť kolena sa môže liečiť doma podľa metód RICE, avšak vážne poranenia kolena môžu vyžadovať okamžitú lekársku pomoc vrátane chiropraktickej starostlivosti.

EXTRA EXTRA | DÔLEŽITÁ TÉMA: Odporúčaný El Paso, TX Chiropraktik
***
Informácie tu uvedené o „Vysvetlenie Nrf2: Cesta Keap1-Nrf2" nie je určený na nahradenie vzťahu jeden na jedného s kvalifikovaným zdravotníckym pracovníkom alebo licencovaným lekárom a nie je to lekárska rada. Odporúčame vám, aby ste rozhodnutia v oblasti zdravotnej starostlivosti robili na základe vášho výskumu a partnerstva s kvalifikovaným zdravotníckym pracovníkom.
Informácie o blogu a diskusie o rozsahu
Náš informačný rozsah sa obmedzuje na chiropraktické, muskuloskeletálne, fyzické lieky, wellness, prispievajúce etiologické viscerozomatické poruchy v rámci klinických prezentácií, súvisiacej somatoviscerálnej reflexnej klinickej dynamiky, subluxačných komplexov, citlivých zdravotných problémov a/alebo článkov, tém a diskusií o funkčnej medicíne.
Poskytujeme a prezentujeme klinická spolupráca so špecialistami z rôznych odborov. Každý špecialista sa riadi svojím odborným rozsahom praxe a jurisdikciou udeľovania licencií. Funkčné zdravotné a wellness protokoly používame na liečbu a podporu starostlivosti o zranenia alebo poruchy pohybového aparátu.
Naše videá, príspevky, témy, predmety a postrehy pokrývajú klinické záležitosti, problémy a témy, ktoré sa týkajú a priamo či nepriamo podporujú náš klinický rozsah praxe.*
Naša kancelária sa primerane pokúsila poskytnúť podporné citácie a identifikovala relevantnú výskumnú štúdiu alebo štúdie podporujúce naše príspevky. Na požiadanie poskytujeme kópie podporných výskumných štúdií, ktoré majú regulačné rady a verejnosť k dispozícii.
Rozumieme, že pokrývame záležitosti, ktoré si vyžadujú ďalšie vysvetlenie, ako môže pomôcť v konkrétnom pláne starostlivosti alebo v protokole liečby; na ďalšiu diskusiu o vyššie uvedenej téme sa preto môžete pokojne opýtať Dr. Alex Jimenez, DC, Alebo kontaktujte nás na adrese 915-850-0900.
Sme tu, aby sme vám a vašej rodine pomohli.
Požehnanie
Dr. Alex Jimenez DC MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
e-mail: coach@elpasofunctionalmedicine.com
Licencovaný ako doktor chiropraxe (DC) v Texas & Nové Mexiko*
Číslo licencie Texas DC TX5807, New Mexico DC Licencia č. NM-DC2182
Licencovaná ako registrovaná zdravotná sestra (RN*) in Florida
Floridská licencia RN licencia # RN9617241 (Kontrola č. 3558029)
Kompaktný stav: Viacštátna licencia: Oprávnený vykonávať prax v Štáty 40*
Dr. Alex Jimenez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Moja digitálna vizitka