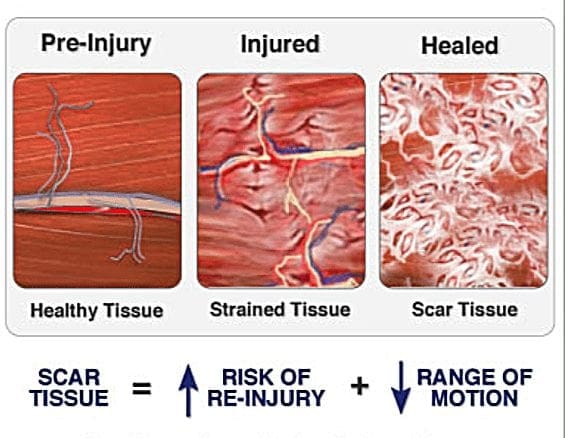
Pain Modulation Pathway Mechanisms v El Paso, TX
Väčšina, ak nie všetky, telesné ochorenia spúšťajú bolesť. Bolesť sa interpretuje a sníma v mozgu. Bolesť je modulovaná dvoma kľúčovými typmi liekov, ktoré pôsobia na mozog: analgetikami a anestetikami. Termín analgetikum sa vzťahuje na liek, ktorý zmierňuje bolesť bez straty vedomia. Výraz centrálna anestézia označuje liek, ktorý tlmí CNS. Vyznačuje sa nedostatočným vnímaním zmyslových modalít, napríklad stratou vedomia bez straty kritických funkcií.
Opiátová analgézia (OA)
Najúspešnejšími klinicky používanými liekmi na vytvorenie dočasnej analgézie a úľavu od bolesti sú opioidné lieky, ktoré zahŕňajú morfín a heroín. V súčasnosti neexistujú žiadne ďalšie účinné možnosti liečby bolesti pre opiáty. Niekoľko vedľajších účinkov spôsobených užívaním opiátov zahŕňa toleranciu a drogovú závislosť alebo závislosť. Vo všeobecnosti tieto lieky okrem dočasného zmiernenia bolesti modulujú informácie o prichádzajúcej bolesti v chrbtici a centrálnom nervovom systéme a možno ich tiež nazývať analgézia produkujúca opiáty (OA). Opiátový antagonista je liek, ktorý antagonizuje opiátové účinky, ako je naloxón alebo maltroxón atď. Sú kompetitívnymi antagonistami opiátových receptorov. Avšak mozog má neurónový okruh a endogénne látky, ktoré modulujú bolesť.
Endogénne opioidy
Opioidergná neurotransmisia sa nachádza v celom mozgu a mieche a predpokladá sa, že ovplyvňuje mnohé funkcie centrálneho nervového systému alebo CNS, ako je nocicepcia, kardiovaskulárne funkcie, termoregulácia, dýchanie, neuroendokrinné funkcie, neuroimunitné funkcie, konzumácia potravy, sexuálna aktivita, súťaživosť. lokomočné správanie, ako aj pamäť a učenie. Opioidy výrazne ovplyvňujú náladu a motiváciu a vyvolávajú pocit eufórie.
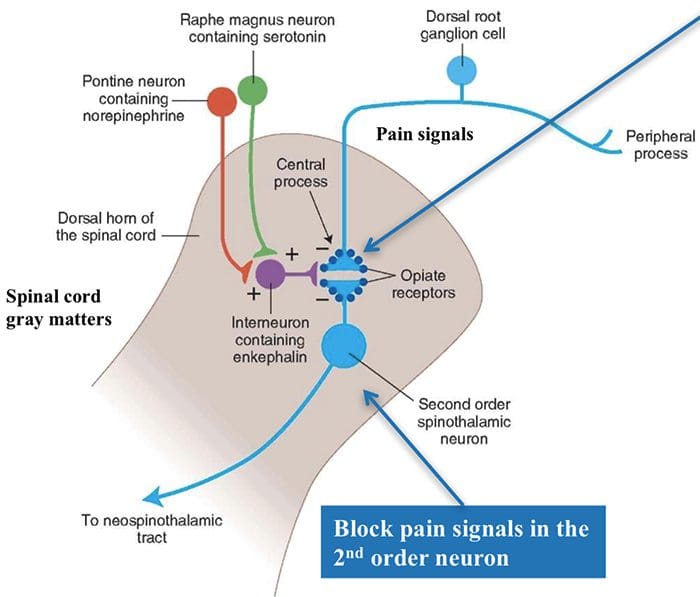
Identifikujú sa tri triedy opioidných receptorov: a-mu, a-delta a a-kappa. Všetky 3 triedy sú široko rozptýlené v mozgu. Gény kódujúce každý z nich boli klonované a zistilo sa, že fungujú ako členovia receptorov G proteínu. Okrem toho boli v centrálnom nervovom systéme rozpoznané tri hlavné typy endogénnych opioidných peptidov, ktoré interagujú s vyššie uvedenými opiátovými receptormi, vrátane a-endorfínov, enkefalínov a dynorfínov. Tieto 3 opioidné peptidy sú odvodené od veľkého proteínového receptora tromi rôznymi génmi, ako je gén proopiomelanokortín alebo POMC, gén proenkefalín a gén prodynorfínu. Opioidné peptidy modulujú nociceptívny vstup dvoma spôsobmi: po prvé, blokujú neurotransmiter uvoľňujú inhibíciou influxu Ca2+ do presynaptického zakončenia, alebo po druhé, otvárajú draslíkové kanály, čo hyperpolarizuje neuróny a inhibuje spike aktivitu. Pôsobia na rôzne receptory v mozgu a mieche.
Enkefalíny sa považujú za predpokladané ligandy pre ? receptory, ? endorfíny pre jeho ?-receptory a dynorfíny pre ? receptory. Rôzne typy opioidných receptorov sú distribuované odlišne v periférnom a centrálnom nervovom systéme alebo v CNS. Existujú dôkazy o funkčných rozdieloch v týchto receptoroch v rôznych štruktúrach. To vysvetľuje, prečo sa po liečbe opiátmi vyskytujú mnohé nežiaduce vedľajšie účinky. Napríklad mu (?) receptory sú rozšírené v parabrachiálnych jadrách mozgového kmeňa, kde dýchacie centrum a inhibícia týchto neurónov môže spôsobiť to, čo je známe ako respiračná depresia.
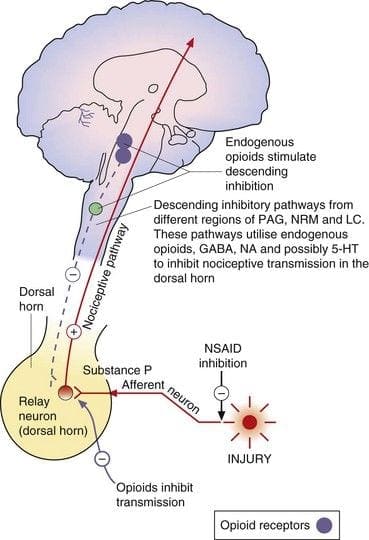
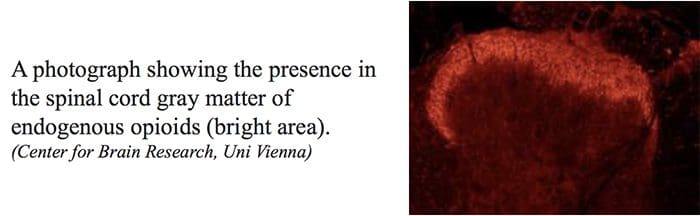
Centrálne alebo periférne zakončenia nociceptívnych aferentných vlákien majú opiátové receptory, v ktorých by exogénne a endogénne opioidy mohli pôsobiť tak, že modulujú schopnosť prenášať nociceptívne informácie. Okrem toho sa vysoké hustoty opiátových receptorov nachádzajú v periakveduktálnej sivej alebo PAG, nucleus raphe magnus alebo NRM a dorzálnej raphe alebo DR, z rostrálnej ventrálnej drene, v mieche, kaudátnom jadre alebo CN, septálnom jadre, hypotalamus, habenula a hippocampus.�Systémovo podávané opioidy v analgetických dávkach aktivujú miechové a supraspinálne mechanizmy prostredníctvom ?, ?, a? typu opioidných receptorov a regulujú signály bolesti, aby modulovali symptómy.
Neurónové okruhy a modulácia bolesti
Po mnoho desaťročí sa predpokladalo, že niekde v centrálnom nervovom systéme existuje okruh, ktorý dokáže modulovať detaily prichádzajúcej bolesti. Teória ovládania brány a vzostupný/zostupný systém prenosu bolesti sú dva návrhy takéhoto okruhu. Nižšie budeme o oboch diskutovať podrobnejšie.
Teória ovládania brány
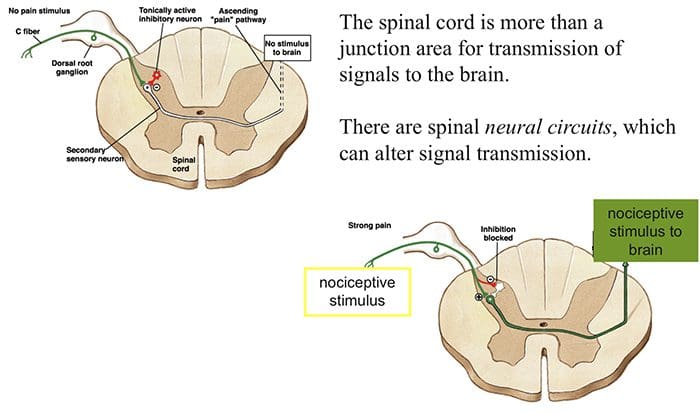
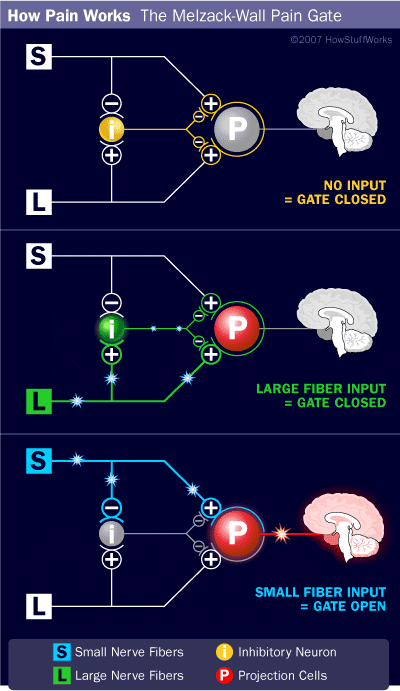
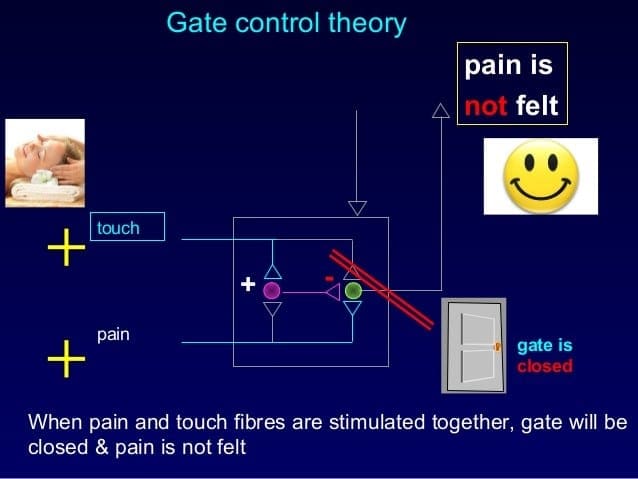
Počiatočný modulačný mechanizmus bolesti známy ako teória ovládania brány, bol navrhnutý Melzackom a Wallom v polovici 1960. rokov XNUMX. storočia. Pojem teórie ovládania brány je taký, že nebolestivý vstup zatvára brány bolestivému vstupu, čo vedie k vyhýbaniu sa pocitu bolesti pri cestovaní do CNS, napríklad neškodlivý vstup alebo stimulácia potláča bolesť.
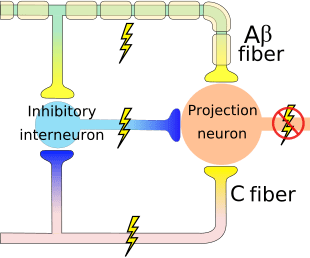
Teória naznačuje, že kolaterály veľkých senzorických vlákien nesúcich kožný senzorický vstup aktivujú inhibičné interneuróny, ktoré inhibujú a regulujú prenos bolesti prenášaný z vlákien bolesti. Neškodlivý vstup potláča bolesť alebo senzorický vstup a zatvára bránu pred škodlivým vstupom. Teória kontroly brány ukazuje, že na úrovni miechy neškodlivá stimulácia vytvorí presynaptickú inhibíciu nociceptorových vlákien dorzálneho koreňa, ktoré sa synapsujú na nociceptorových miechových neurónoch (T). Táto presynaptická inhibícia tiež zabráni tomu, aby sa prichádzajúce škodlivé informácie dostali do CNS, napríklad zatvorí bránu pre prichádzajúce toxické informácie.
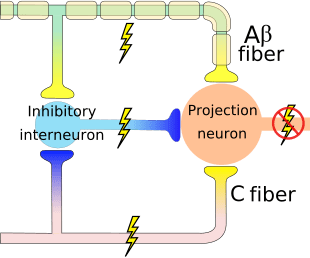
Teória kontroly brány bola zdôvodnením myšlienky výroby a využitia transkutánnej elektrickej nervovej stimulácie alebo TENS na úľavu od bolesti. Aby bola jednotka TENS účinná, generuje dve rôzne aktuálne frekvencie pod prahom bolesti, ktoré môže pacient prijať. Tento proces našiel určitý stupeň úspechu v liečbe chronickej bolesti.
Modulácia bolesti: Teória kontroly brány
Analgézia vyvolaná stimuláciou (SPA)
Dôkazy o inherentnom analgetickom systéme sa našli intrakraniálnou elektrickou stimuláciou určitých diskrétnych oblastí mozgu. Týmito oblasťami by boli periakveduktálne šedé alebo PAG a nucleus raphe magnus alebo NRM, dorzálne raphe alebo DR, caudate nucleus alebo CN, septálne jadro alebo Spt, spolu s inými jadrami. Takáto stimulácia alebo zmyslové signály potláčajú bolesť, pričom vyvolávajú analgéziu bez potlačenia správania, pričom pocit dotyku, teploty a tlaku zostáva nedotknutý. Podľa výskumných štúdií je SPA alebo stimulácia vyvolaná analgézia výraznejšia a trvá dlhšie po stimulácii u ľudí ako u pokusných zvierat. Okrem toho počas SPA subjekty stále reagujú na nebolestivú stimuláciu, ako je teplota a dotyk v ohraničenej oblasti analgézie. Najúčinnejšie oblasti CNS alebo centrálneho nervového systému pre výskyt SPA by boli v PAG a raphe nuclei alebo RN.
Elektrická stimulácia PAG alebo NRM inhibuje miechové talamické bunky alebo miechové neuróny, ktoré vyčnievajú monosynapticky do talamu, v laminách I, II a V, aby sa zabezpečili škodlivé informácie z nociceptorov, ktoré sú v konečnom dôsledku modulované na úrovni miechy. Okrem toho má PAG neurónové spojenia s nucleus raphe magnus alebo NRM.
K aktivite PAG s najväčšou pravdepodobnosťou dochádza aktiváciou zostupnej dráhy z NRM a pravdepodobne aj aktiváciou vzostupných spojení pôsobiacich na vyšších subkortikálnych úrovniach CNS. Okrem toho elektrická stimulácia PAG alebo NRM produkuje behaviorálnu analgéziu alebo stimuláciu produkovanú analgéziu. Stimuláciou vyvolaná analgézia alebo SPA spôsobuje uvoľňovanie endorfínov, ktoré môže blokovať opiátový antagonista naloxón.
Počas stimulácie PAG a/alebo RN môže byť serotonín, v medicíne tiež označovaný ako 5-HT, vylučovaný zo vzostupných a zostupných axónov zo subkortikálnych jadier, v miechových trigeminálnych jadrách a v mieche. Toto uvoľňovanie 5-HT moduluje a reguluje prenos bolesti inhibíciou alebo blokovaním prichádzajúcej nervovej činnosti. Deplécia 5-HT elektrickou léziou jadier raphe alebo neurotoxickou léziou vytvorenou lokálnou injekciou chemického činidla, ako je parachlórfenylalanín alebo PCPA, vedie k blokovaniu sily opiátu, intrakraniálnej aj systémovej, ako aj sily opiátu. elektrická stimulácia s cieľom vyvolať analgéziu.
Aby sa potvrdilo, či elektrická stimulácia vyvolala analgéziu prostredníctvom uvoľnenia opiátu a dopamínu, potom sa do oblasti lokálne mikroinjektuje morfín alebo 5-HT. Všetky tieto mikroinjekcie v konečnom dôsledku vytvárajú analgéziu. Tieto procesy tiež poskytujú spôsob identifikácie oblastí mozgu súvisiacich s potláčaním bolesti a pomáhajú vytvárať mapu centier bolesti. Najúčinnejším spôsobom produkcie opiátovej analgézie alebo OA je intracerebrálna injekcia morfínu do PAG.
PAG a RN, ako aj iné mozgové štruktúry, v ktorých sa produkuje analgézia, sú tiež bohaté na opiátové receptory. Intracerebrálne podávanie opioidov vyvolávajúce analgéziu a SPA možno blokovať systémovými alebo lokálnymi mikroinjekciami naloxónu, antagonistu morfínu, do PAG alebo RN. Z tohto dôvodu sa navrhuje, aby obe, OA aj SPA, fungovali častým mechanizmom.
Ak sa OA a SPA správajú prostredníctvom rovnakého vnútorného systému, potom je oveľa pravdepodobnejšia hypotéza, že opiáty aktivujú mechanizmus potláčania bolesti. V skutočnosti súčasné dôkazy naznačujú, že mikroinjekcie opiátu do PAG aktivujú eferentný systém mozgového kmeňa, ktorý inhibuje prenos bolesti na úrovni segmentovej miechy. Tieto pozorovania naznačujú, že analgézia vyvolaná z periaqueduktálnej šedej alebo PAG vyžaduje zostupnú dráhu do miechy.

Pohľad Dr. Alexa Jimeneza
K modulácii bolesti dochádza prostredníctvom procesu elektrickej stimulácie mozgu, ku ktorej dochádza v dôsledku aktivácie zostupných inhibičných vlákien, ktoré regulujú alebo inhibujú vstup a výstup určitých neurónov. Predpokladá sa, že to, čo bolo opísané ako opioidné a serotonergné antagonisty, zvráti lokálnu opiátovú analgéziu aj analgéziu generovanú mozgovými stimulmi. Senzorické signály alebo impulzy v centrálnom nervovom systéme sú v konečnom dôsledku kontrolované vzostupnými aj zostupnými inhibičnými systémami, pričom ako inhibičné mediátory sa využívajú endogénne opioidy alebo iné endogénne látky, ako je serotonín. Bolesť je komplexné vnímanie, ktoré môže byť ovplyvnené aj množstvom iných faktorov, vrátane emocionálneho stavu.
Mechanizmy modulácie bolesti
Vzostupný a zostupný mechanizmus potláčania bolesti
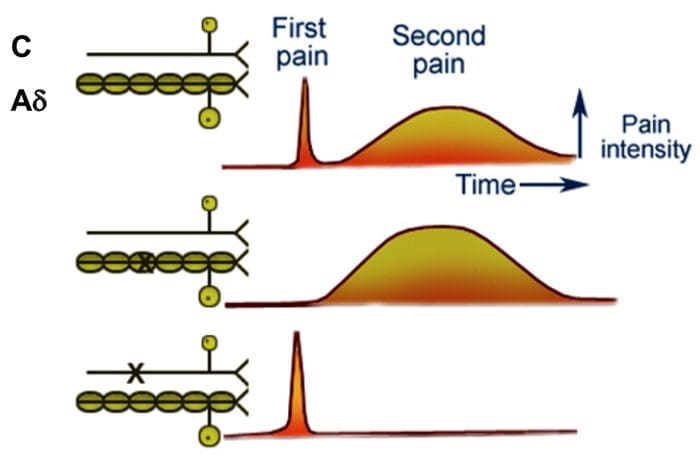
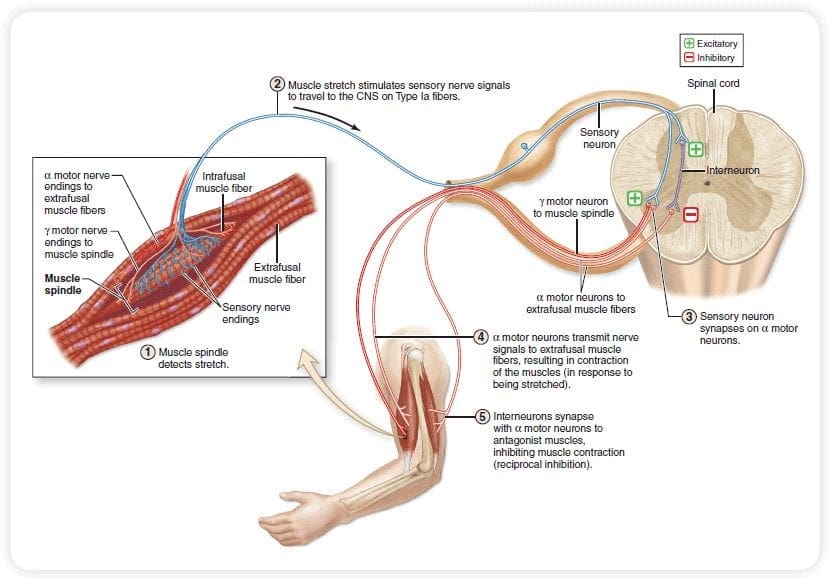
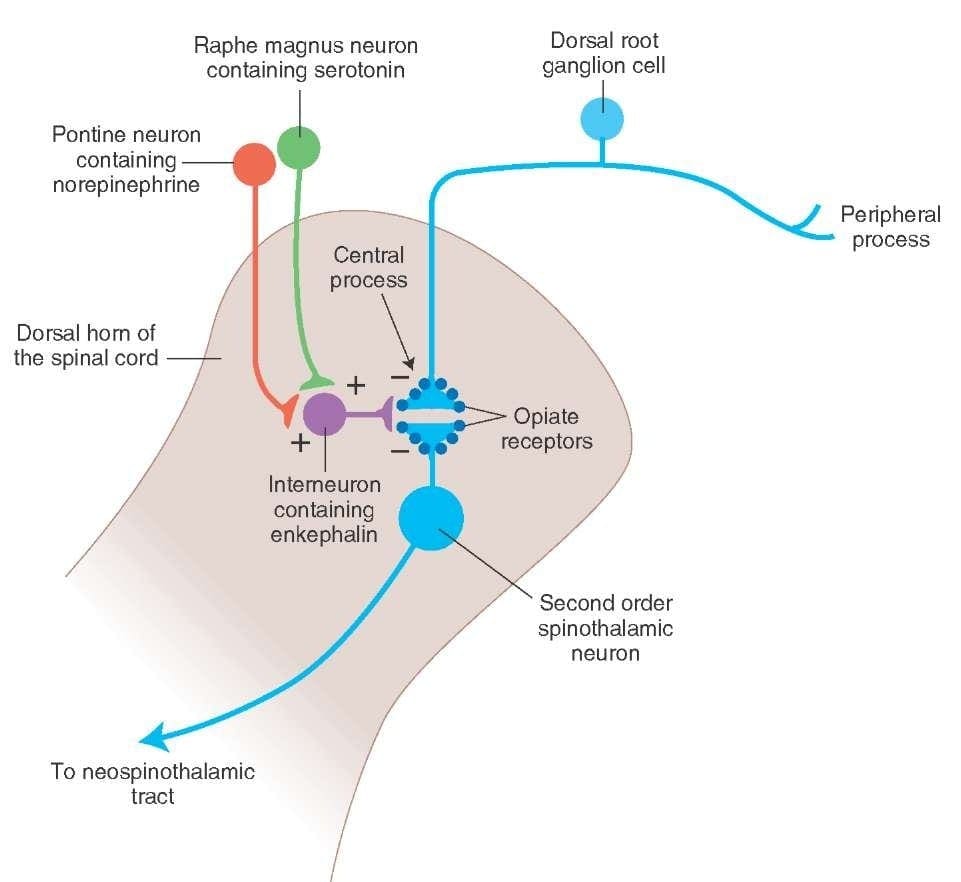
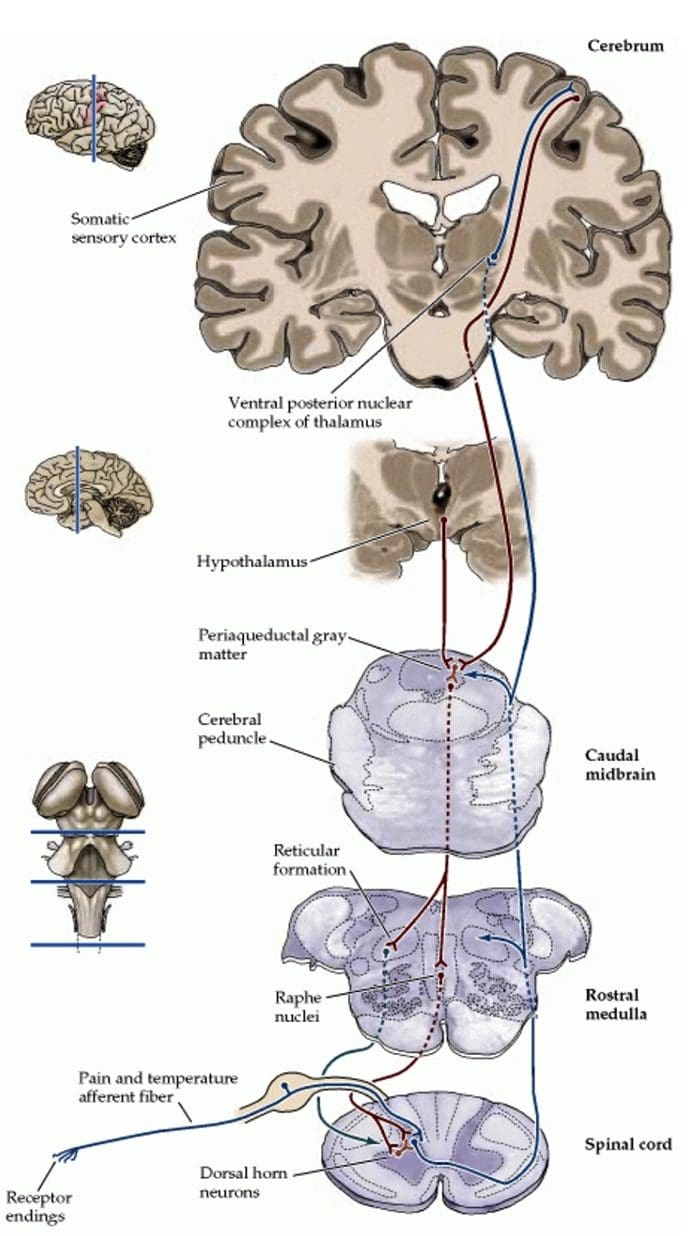
Primárne vlákna vzostupnej bolesti, ako napríklad A? a C vlákna, dosahujú dorzálny roh miechy z periférnych nervových oblastí, aby inervovali nociceptorové neuróny v Rexed laminae I & II. Bunky z Rexed lamina II vytvárajú synaptické spojenia v Rexedových vrstvách IV až VII. Bunky, najmä v laminách I a VII dorzálneho rohu, spôsobujú vzostupný spinothalamický trakt. Na miechovej úrovni sú opiátové receptory umiestnené v presynaptických zakončeniach ich nocineurónov a vo vrstvách IV až VII interneurálnej úrovne od dorzálneho rohu.
Aktivácia opiátových receptorov na interneuronálnej úrovni spôsobuje hyperpolarizáciu neurónov, čo vedie k inhibícii aktivácie, ako aj k uvoľňovaniu substancie P, neurotransmiteru zapojeného do prenosu bolesti, čím sa bráni prenosu bolesti. Okruh, ktorý pozostáva z periakvaduktálnej šedej alebo PAG hmoty v hornom mozgovom kmeni, locus coeruleus alebo LC, nucleus raphe magnus alebo NRM a nucleus reticularis gigantocellularis alebo Rgc, vedie k zostupnej bolesti. supresívna dráha, ktorá inhibuje prichádzajúce údaje o bolesti na úrovni miechy.
Ako už bolo uvedené, opioidy interagujú s opiátovými receptormi na rôznych úrovniach centrálneho nervového systému. Tieto opiátové receptory sú normálnymi cieľovými oblasťami pre hormóny a endogénne opiáty, ako sú endorfíny a enkefalíny. V dôsledku väzby na receptor v subkortikálnych webových stránkach dochádza k sekundárnym zmenám, ktoré vedú k určitej zmene v elektrofyziologických vlastnostiach neurónov a regulácii ich vzostupnej informácie o bolesti.
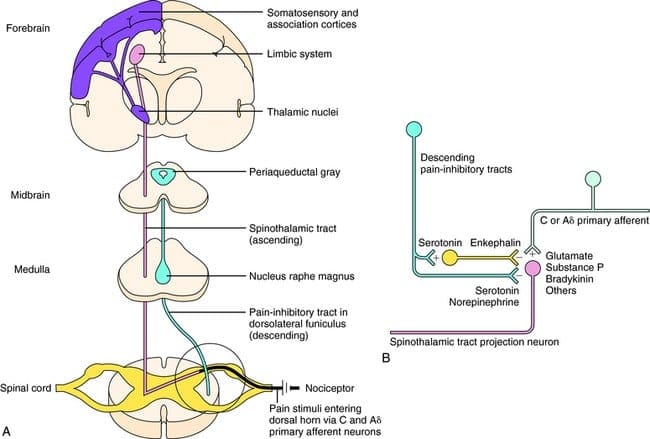
Čo aktivuje PAG, aby uplatnila svoje dôsledky? Zistilo sa, že škodlivá stimulácia spúšťa neuróny v nucleus reticularis gigantocellularis alebo RGC. Jadro Rgc inervuje PAG aj NRM. PAG posiela axóny do NRM a nervy v NRM posielajú svoje axóny do miechy. Okrem toho bilaterálne dorzolaterálne lézie funiculus alebo DLF, označované ako DLFX, blokujú analgéziu produkovanú elektrickou stimuláciou a mikroinjekciou opiátov priamo do PAG a NRM, ale len zmierňujú systémové analgetické účinky opiátov. Tieto pozorovania podporujú hypotézu, že diskrétne zostupné dráhy z DLF sú potrebné pre OA aj SPA.
DLF sa skladá z vlákien pochádzajúcich z niekoľkých jadier mozgového kmeňa, ktoré môžu byť serotonergné alebo 5-HT, z nervov umiestnených vo vnútri nucleus raphe magnus alebo NRM; dopaminergné neuróny pochádzajúce z ventrálnej tegmentálnej oblasti alebo VTA a adrenergné neuróny pochádzajúce z locus coeruleus alebo LC. Tieto zostupné vlákna potláčajú škodlivý vstup do nociceptívnych neurónov miechy v laminách I, II a V.
Opiátové receptory boli tiež objavené v dorzálnom rohu miechy, hlavne v Rexed laminae I, II a V, a takéto spinálne opiátové receptory sprostredkúvajú inhibičné účinky na neuróny dorzálneho rohu prenášajúce nociceptívne informácie. Zdá sa, že účinok morfínu sa uplatňuje rovnako v mieche a jadrách mozgového kmeňa, vrátane PAG a NRM. Systémový morfín pôsobí na opiátové receptory mozgového kmeňa aj miechy a vyvoláva analgéziu. Morfín sa viaže na opiátové receptory mozgového kmeňa, čo spúšťa zostupnú serotonergnú dráhu mozgového kmeňa do miechy, ako aj DLF, a tieto majú opioidmi sprostredkovanú synapsiu na úrovni miechy.
Toto pozorovanie demonštruje, že škodlivé stimuly namiesto neškodlivého stimulu určujú teóriu kontroly brány, ktorá je kritická pre aktiváciu zostupného okruhu modulácie bolesti, kde bolesť inhibuje bolesť prostredníctvom zostupnej dráhy DLF. Okrem toho existujú vzostupné spojenia v PAG a jadrách raphe do komplexu PF-CM. Tieto oblasti talamu sú súčasťou vzostupnej modulácie bolesti na stupni diencefala.
Analgézia vyvolaná stresom (SIA)
Analgézia sa môže objaviť za určitých stresových okolností. Vystavenie mnohým rôznym stresujúcim alebo bolestivým udalostiam vytvára analgetickú odpoveď. Tento jav je známy ako stresom indukovaná analgézia alebo SIA. Predpokladá sa, že analgézia vyvolaná stresom poskytuje pohľad na fyziologické a psychologické faktory, ktoré spúšťajú endogénne systémy kontroly bolesti a opiátové systémy. Napríklad vojaci zranení v bitke alebo zranení športovci pri športe niekedy uvádzajú, že počas bitky alebo hry necítia bolesť alebo nepohodlie, napriek tomu prejdú bolesťou potom, čo sa špecifická situácia zastaví. Na zvieratách bolo dokázané, že elektrické šoky spôsobujú stresom indukovanú analgéziu. Na základe týchto experimentov sa predpokladá, že tlak, ktorý zažívali vojaci a športovci, potláčal bolesť, ktorú neskôr zažili.
Predpokladá sa, že endogénne opiáty sú produkované ako odpoveď na stres a inhibujú bolesť spustením zostupného systému stredného mozgu. Okrem toho niektoré SIA vykazovali skríženú toleranciu s opiátovou analgéziou, čo naznačuje, že tento SIA je sprostredkovaný cez opiátové receptory. Experimenty využívajúce rôzne parametre stimulácie elektrickým šokom demonštrujú takúto stresom indukovanú analgéziu a niektoré z tých úzkostí, ktoré vyvolávajú analgéziu, by mohli byť blokované opioidným antagonistom naloxónom, zatiaľ čo iné neboli blokované naloxónom. Na záver, tieto pozorovania vedú k rozhodnutiu, že existujú opiátové aj neopiátové formy SIA.
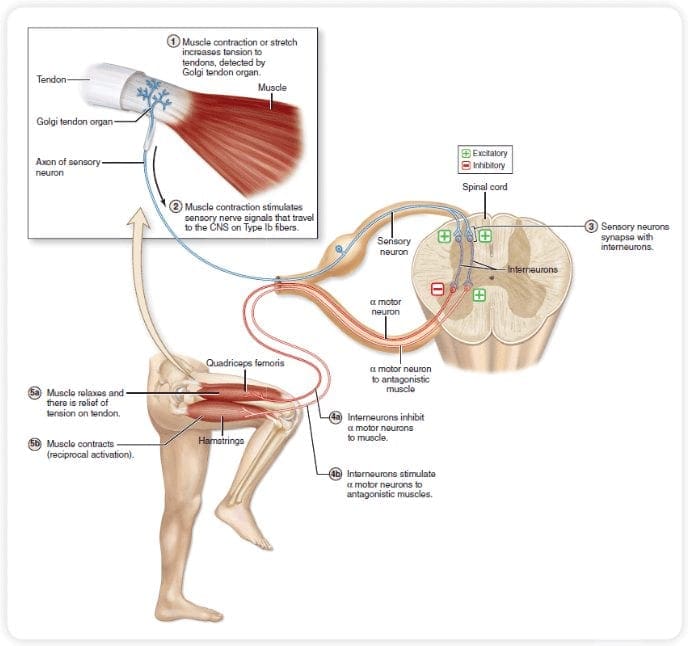
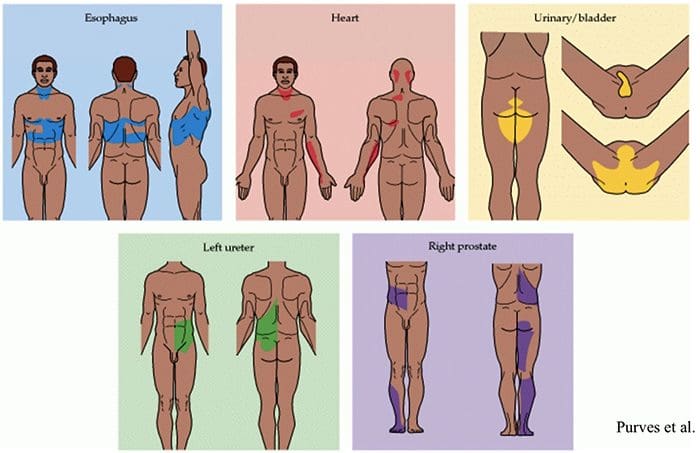
Somatoviscerálny reflex
Somatoviscerálny reflex je reflex, pri ktorom sú viscerálne funkcie aktivované alebo inhibované somatickou senzorickou stimuláciou. U pokusných zvierat je dokázané, že škodlivá aj neškodná stimulácia somatických aferentov vyvoláva reflexné zmeny v eferentnej aktivite sympatiku a následne vo funkcii efektorových orgánov. Tieto javy boli preukázané v takých oblastiach, ako je gastrointestinálny trakt, močové cesty, dreň nadobličiek, lymfatické bunky, srdce a cievy mozgu a periférne nervy.
Najčastejšie sa rezy vyvolávajú experimentálne stimuláciou kožných aferentných kanálov, aj keď niektoré práce sa vykonali aj na svalových a artikulárnych aferentoch, vrátane miechových buniek. Konečné reakcie budú predstavovať integráciu viacerých tonických a reflexných vplyvov a môžu vykazovať laterálne a segmentové trendy, ako aj premenlivú excitabilitu v súlade so zapojenými aferentáciami. Vzhľadom na zložitosť a mnohopočetnosť mechanizmov zapojených do posledného vyjadrenia reflexnej odpovede, pokusy o extrapoláciu na klinické situácie by sa mali s najväčšou pravdepodobnosťou uskutočniť v prospech ďalších systematických fyziologických štúdií.
Rozsah našich informácií je obmedzený na chiropraktiku, ako aj na poranenia a stavy chrbtice. Ak chcete prediskutovať túto tému, neváhajte sa opýtať Dr. Jimeneza alebo nás kontaktujte na adrese 915-850-0900 .
Kurátorom je Dr. Alex Jimenez
Ďalšie témy: Ischias
ischias sa v medicíne označuje ako súbor symptómov, a nie ako jediné zranenie a/alebo stav. Symptómy bolesti sedacieho nervu alebo ischias sa môžu líšiť frekvenciou a intenzitou, najčastejšie sa však opisuje ako náhla, ostrá (nožovitá) alebo elektrická bolesť, ktorá vyžaruje z dolnej časti chrbta do zadku, bokov, stehien a nohy do chodidla. Ďalšie príznaky ischias môžu zahŕňať pocity brnenia alebo pálenia, necitlivosť a slabosť po celej dĺžke sedacieho nervu. Ischias najčastejšie postihuje jedincov vo veku 30 až 50 rokov. Často sa môže vyvinúť ako dôsledok degenerácie chrbtice vekom, avšak stlačenie a podráždenie sedacieho nervu spôsobené vydutím resp. herniovaný disk, okrem iných zdravotných problémov chrbtice, môže tiež spôsobiť bolesť sedacieho nervu.

EXTRA DÔLEŽITÁ TÉMA: Chiropraktik Symptómy ischias



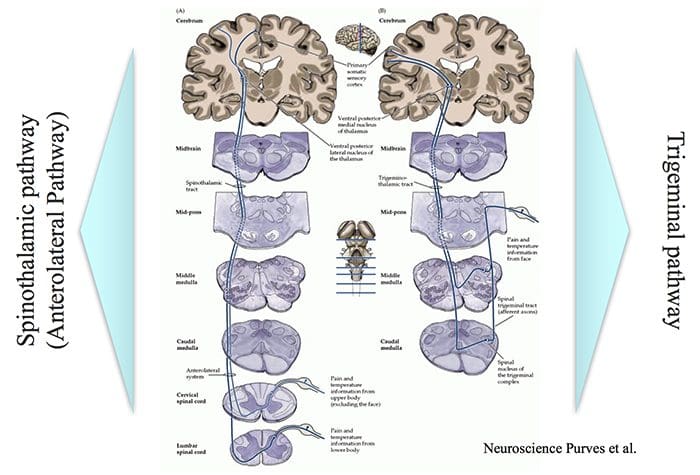
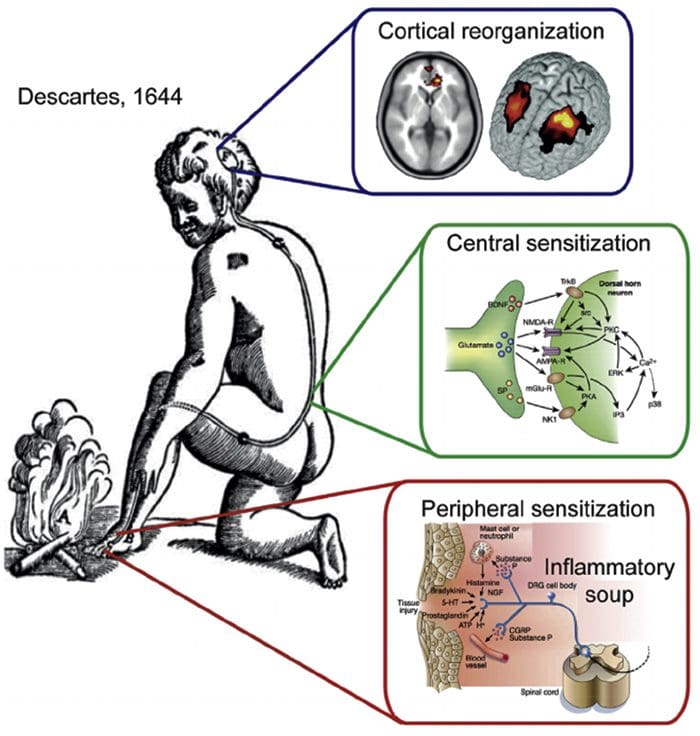
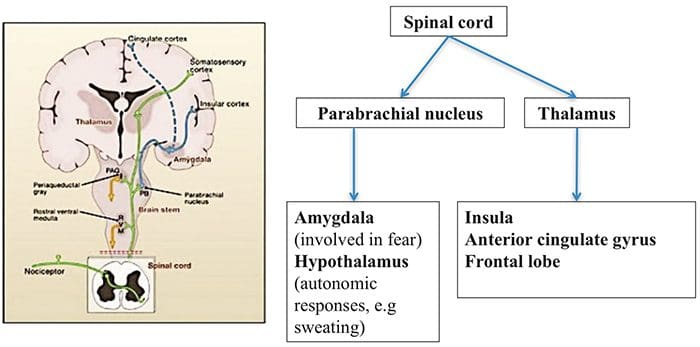 Oblasti mozgu zapojené do spracovania nociceptívnych signálov
Oblasti mozgu zapojené do spracovania nociceptívnych signálov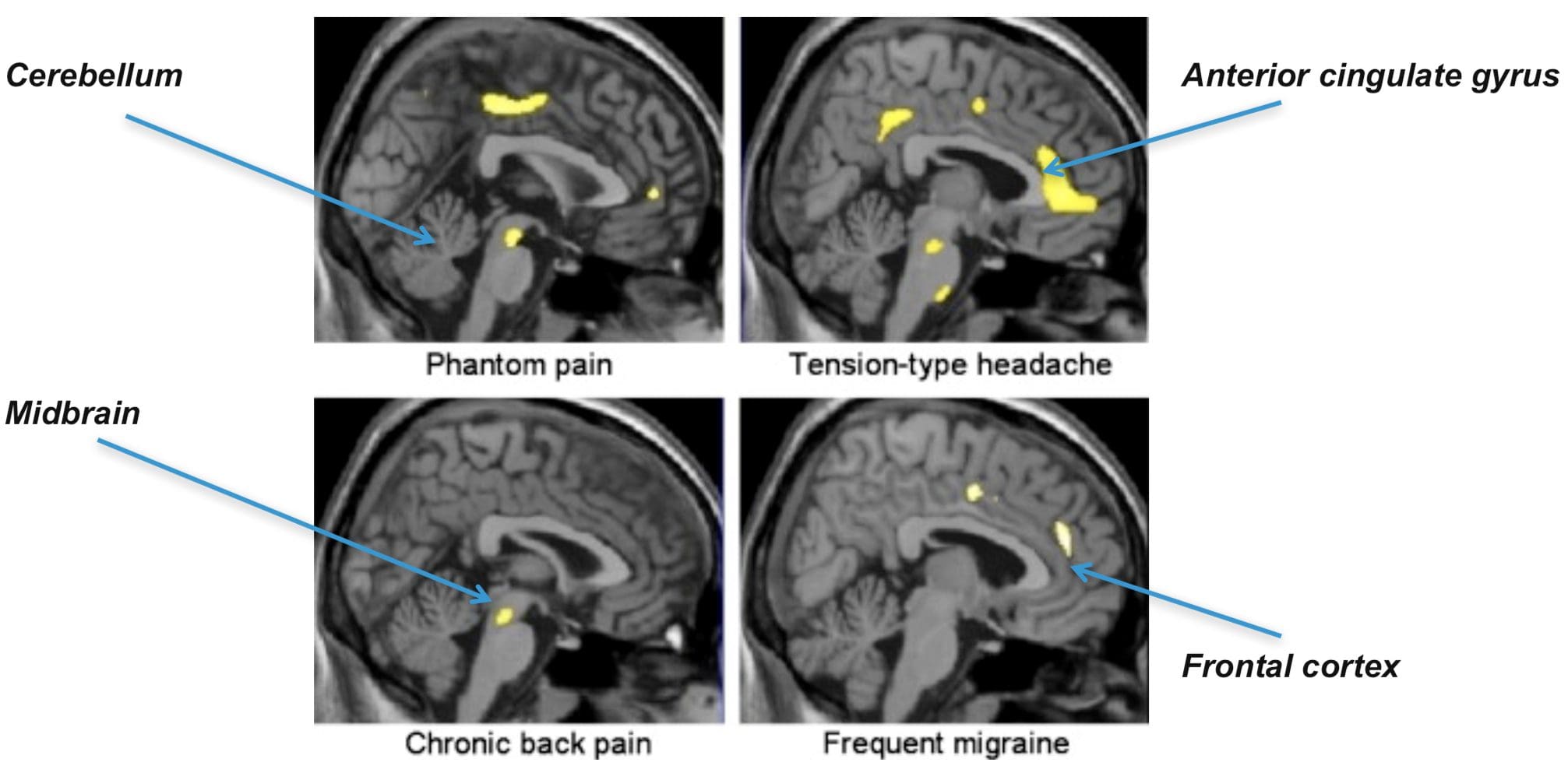 Predný cingulát a kôra ostrovčeka sa aktivujú u ľudských subjektov
Predný cingulát a kôra ostrovčeka sa aktivujú u ľudských subjektov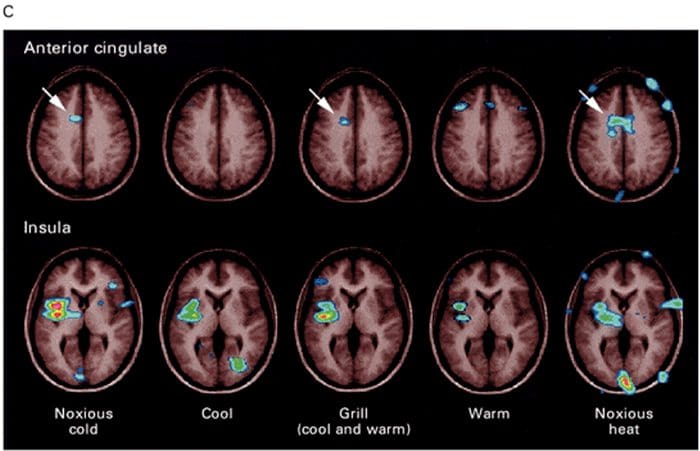
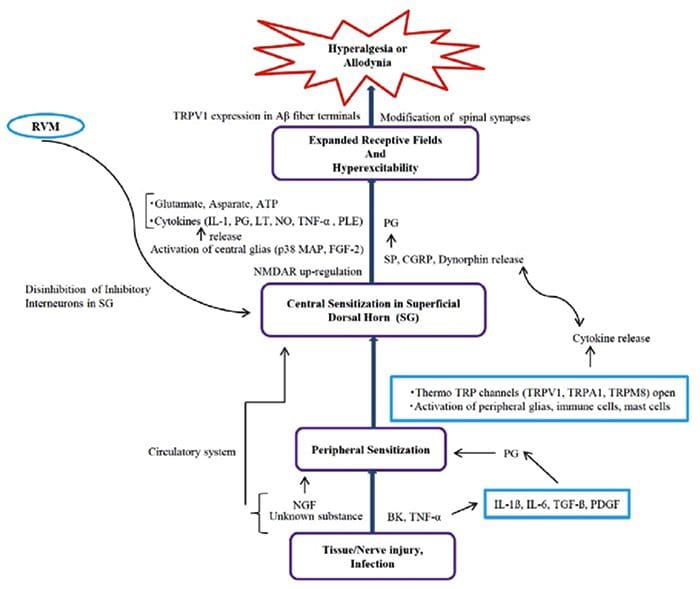
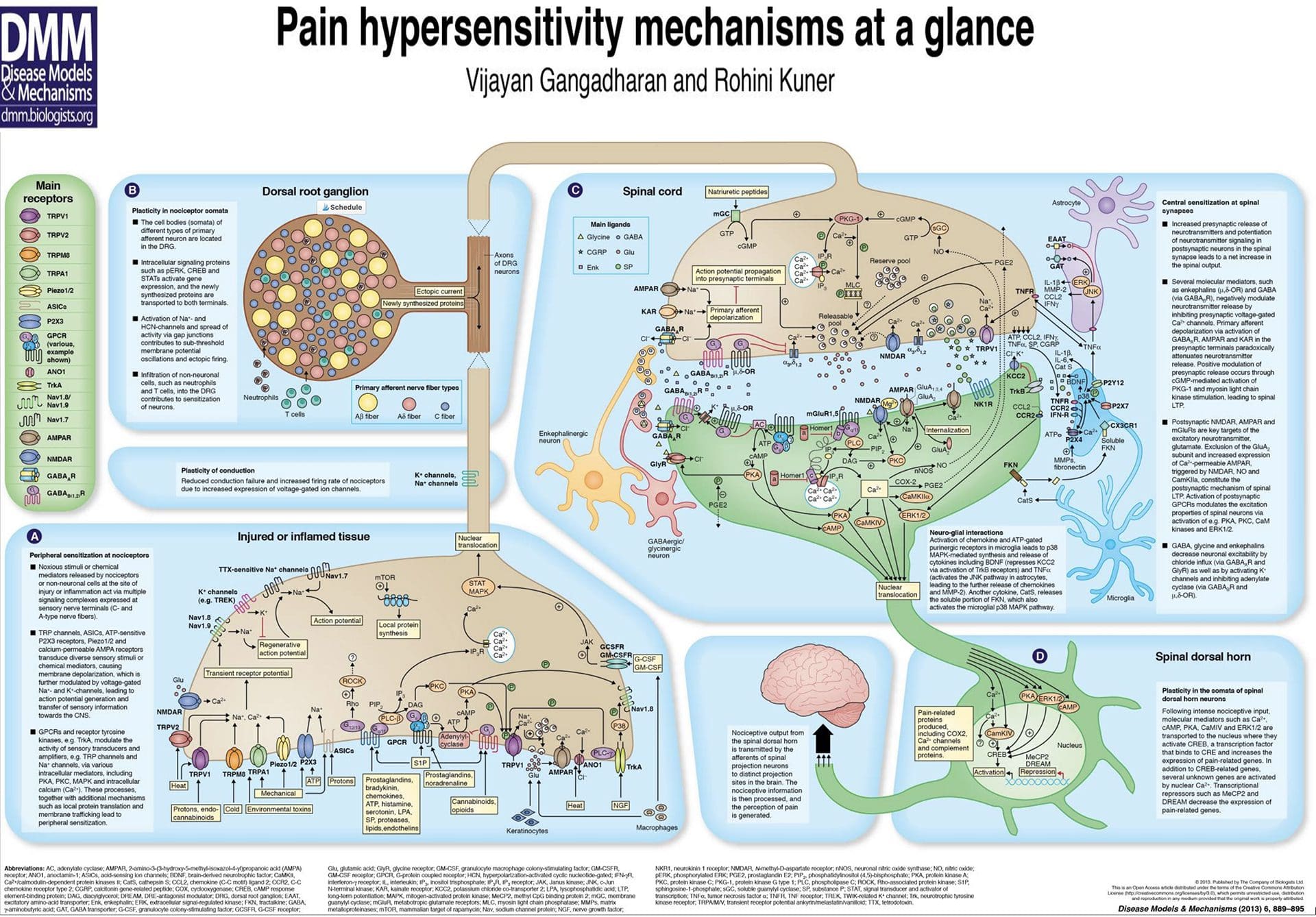
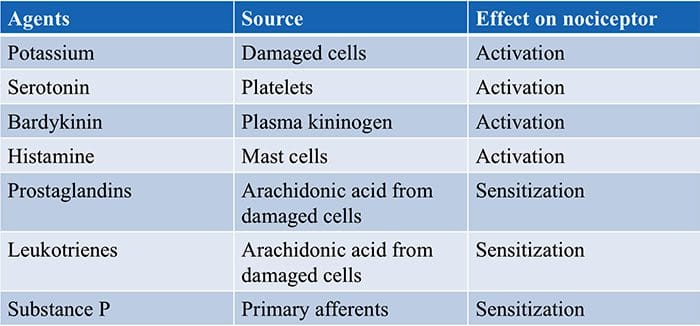
 Zápalová polievka – hyperalgézia
Zápalová polievka – hyperalgézia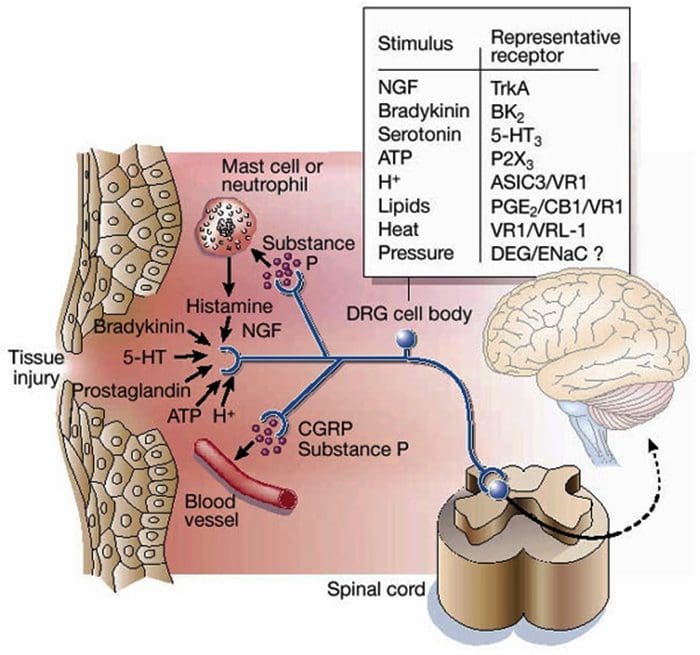
 Gate Control Theory of Pain
Gate Control Theory of Pain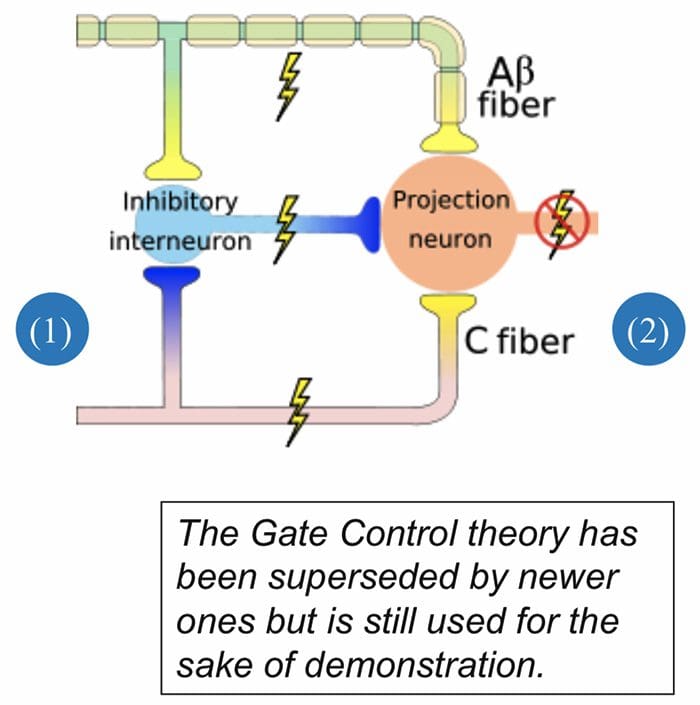
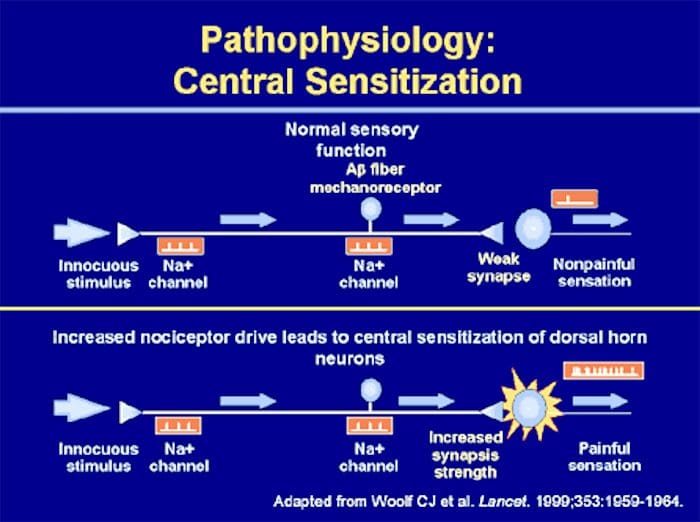
 Abnormality systému bolesti
Abnormality systému bolesti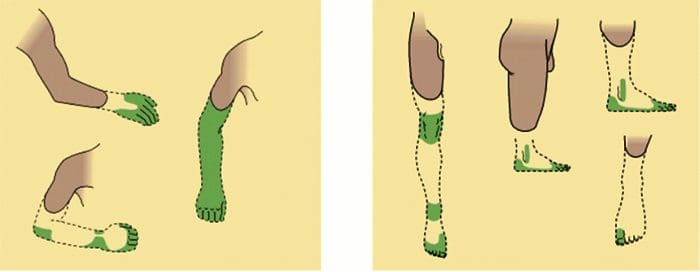 Periférna senzibilizácia
Periférna senzibilizácia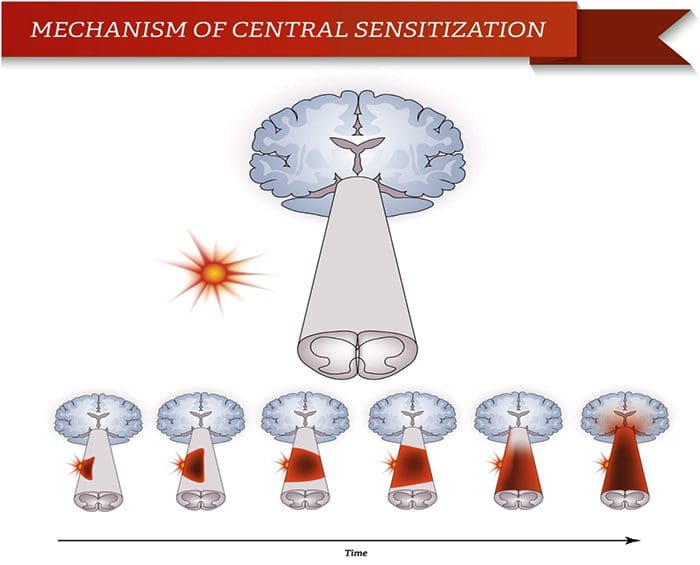
 Organizácia somatosenzorickej kôry
Organizácia somatosenzorickej kôry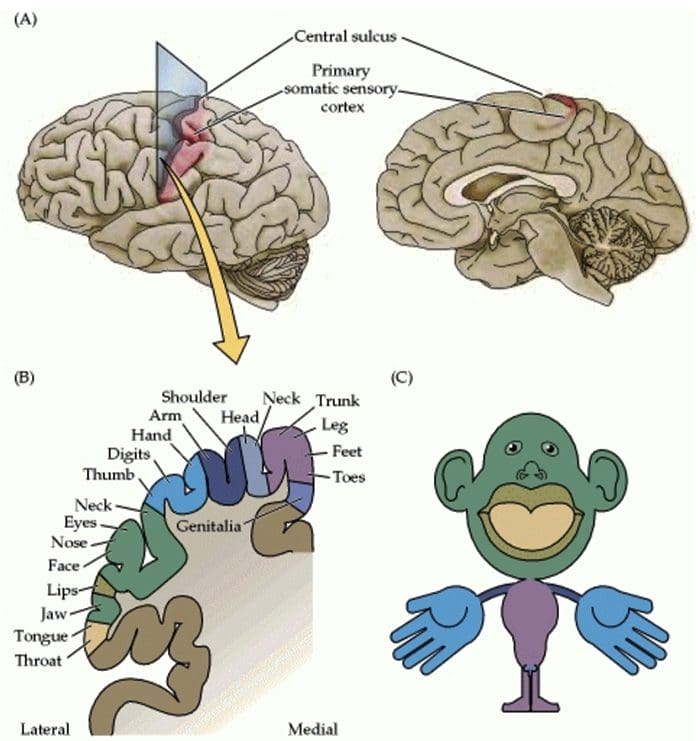 Kortikálna reorganizácia
Kortikálna reorganizácia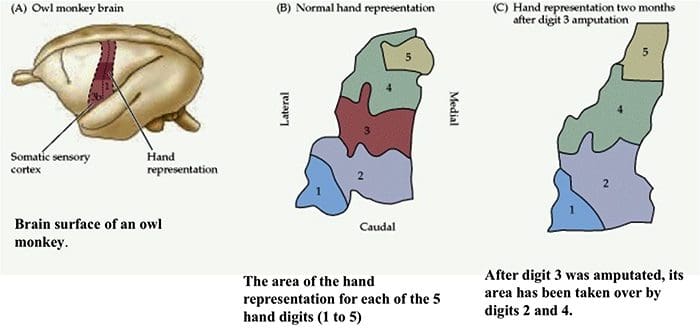

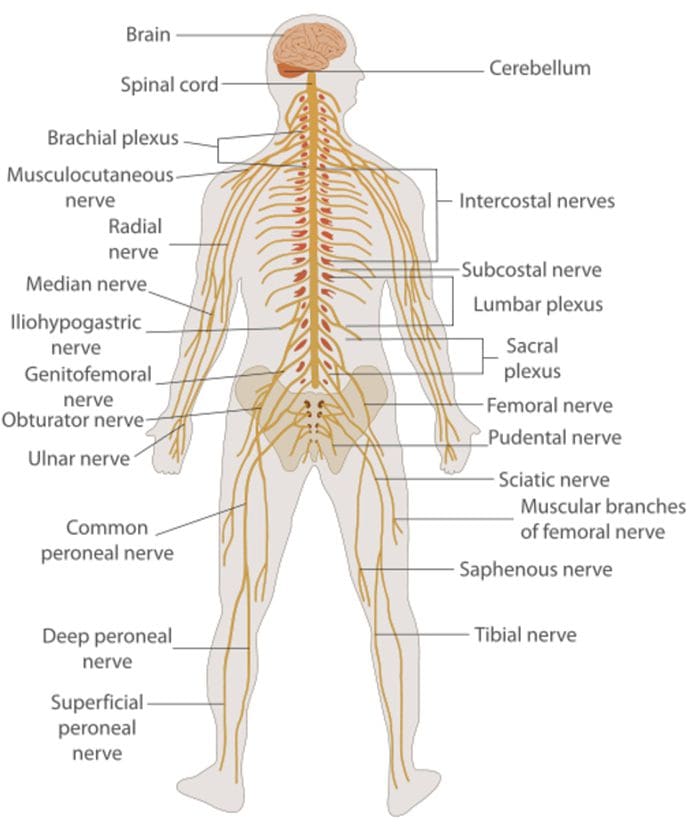
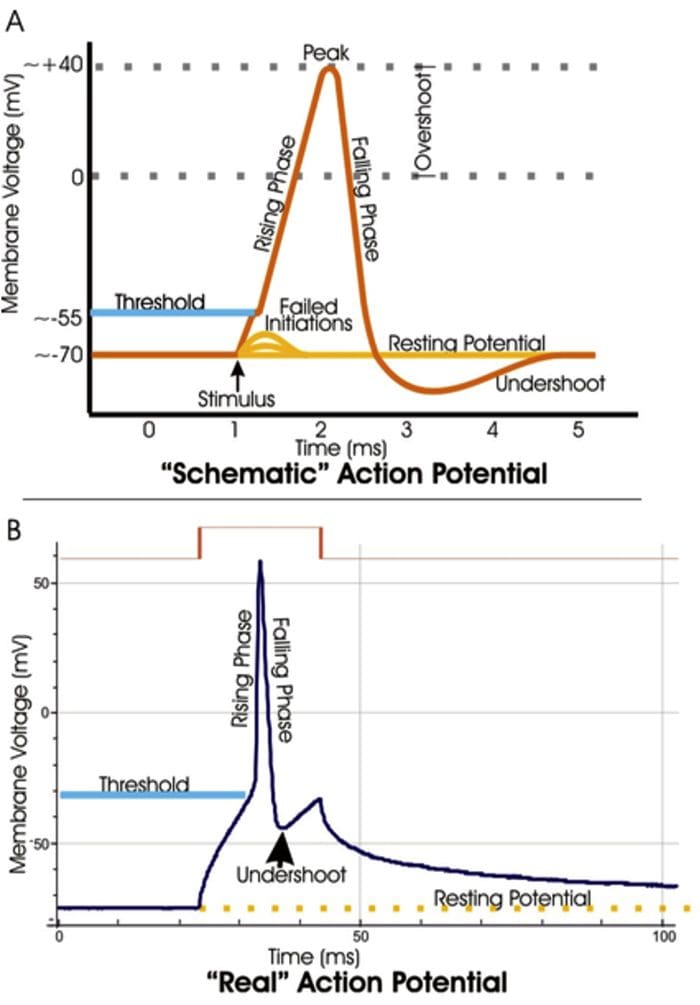
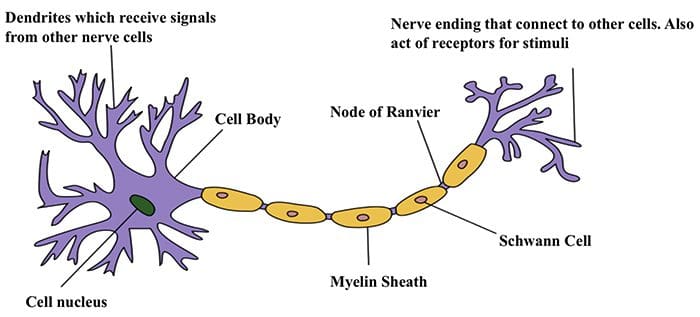 Komunikácia medzi nervovou bunkou
Komunikácia medzi nervovou bunkou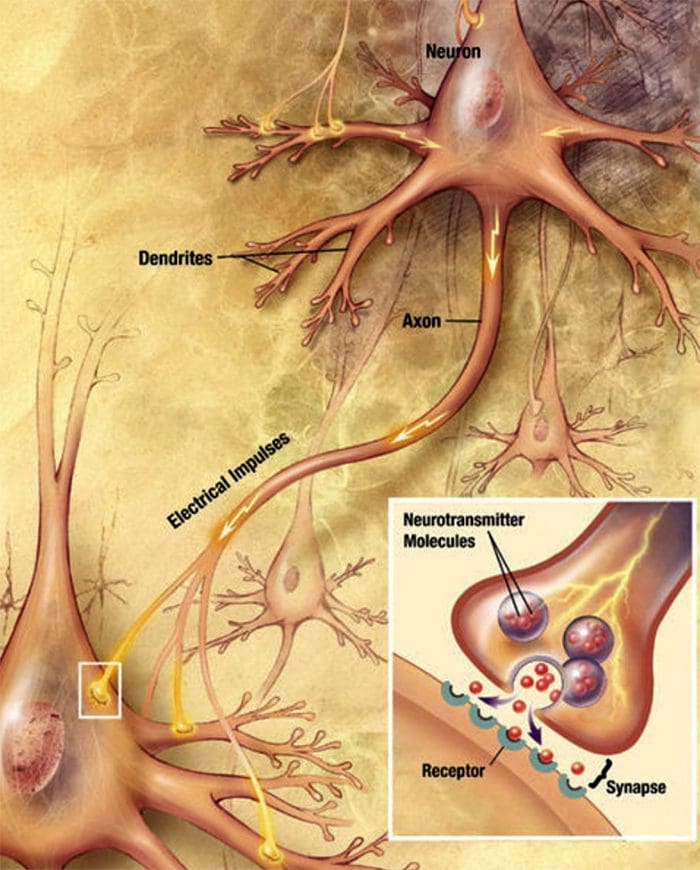 Nervové bunky komunikujú s inými bunkami uvoľňovaním chemikálie z nervových zakončení � Neurotransmitery
Nervové bunky komunikujú s inými bunkami uvoľňovaním chemikálie z nervových zakončení � Neurotransmitery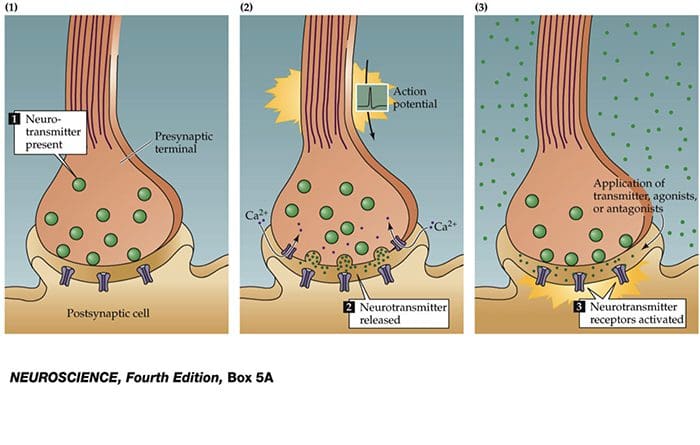
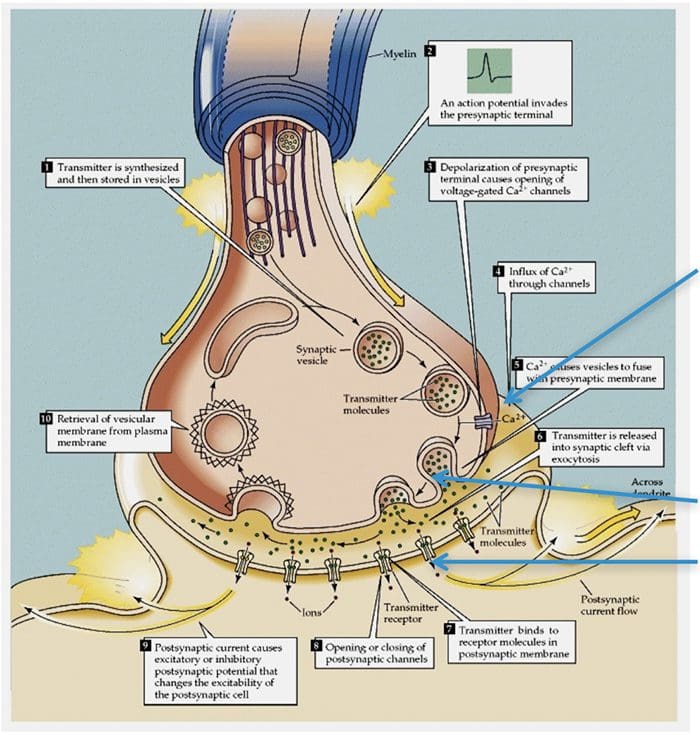
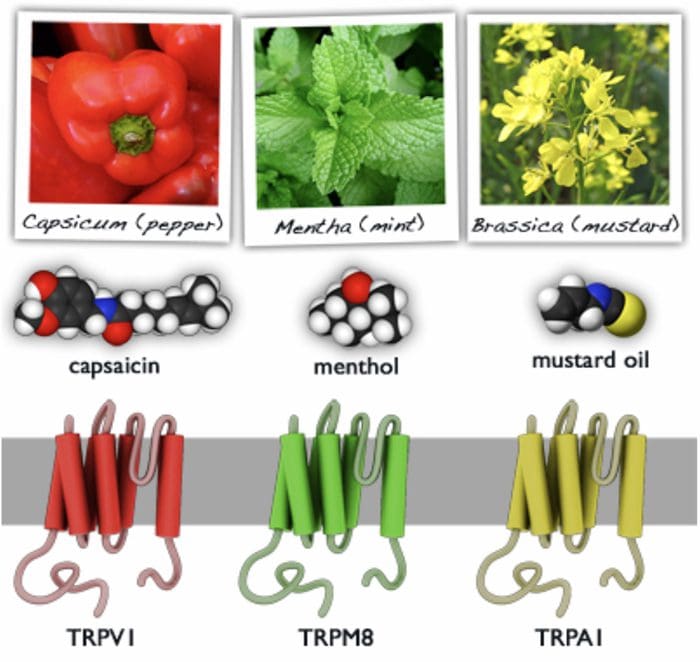
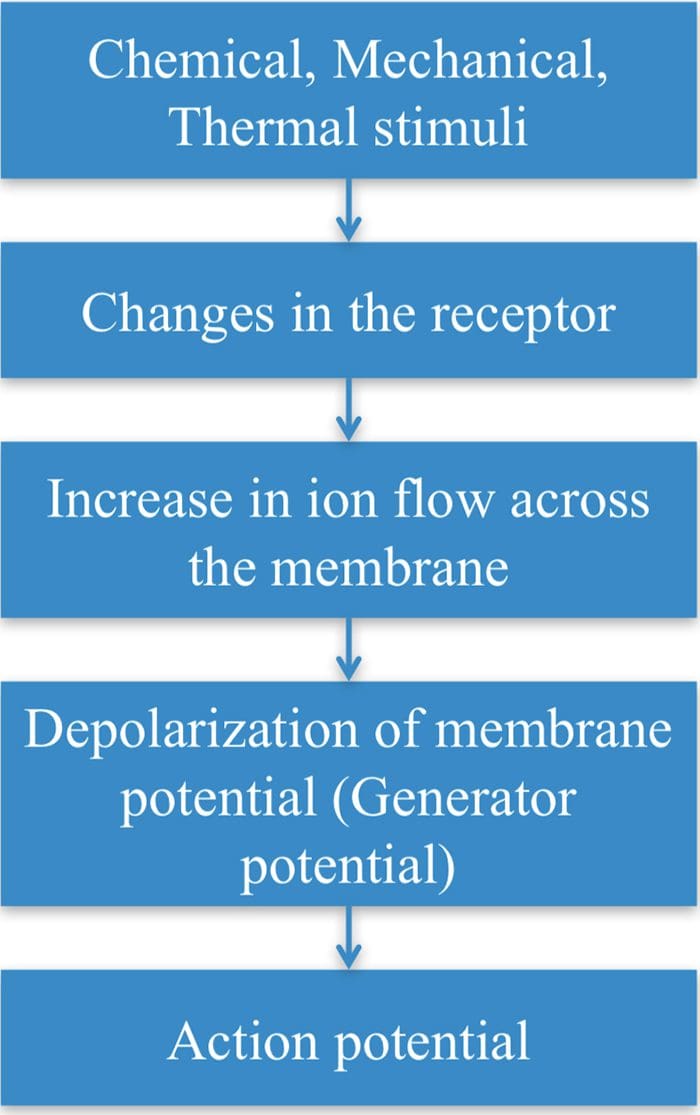 TRP kanály
TRP kanály